多抗亲和层析纯化
多抗亲和层析纯化技术
一、技术简介
多抗亲和层析纯化技术是基于抗原 - 抗体特异性结合原理建立的高效蛋白质分离技术。通过将目标抗原或抗体共价偶联到层析介质(如琼脂糖凝胶、磁性微球)表面作为配基,当含多克隆抗体的复杂生物样品(血清 / 腹水 / 细胞上清)流经层析柱时,目标抗体通过 Fab 段与配基特异性结合,而杂蛋白(白蛋白、细胞因子等)随流动相排出。通过优化洗脱条件(酸性缓冲液 / 高盐溶液 / 竞争性抗原)破坏抗原 - 抗体相互作用,可精准洗脱高纯度多克隆抗体(纯度≥95%),实现从复杂体系中一步法分离目标抗体。
二、技术优势
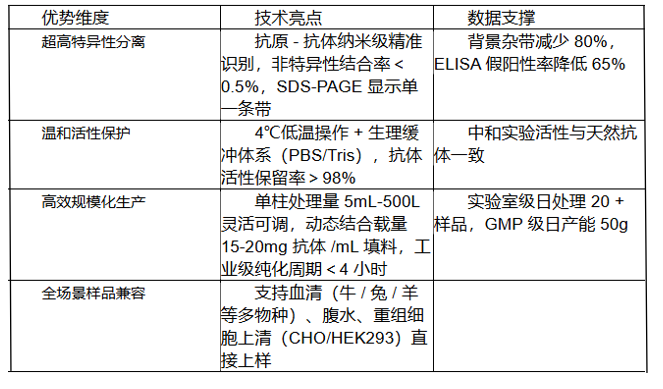
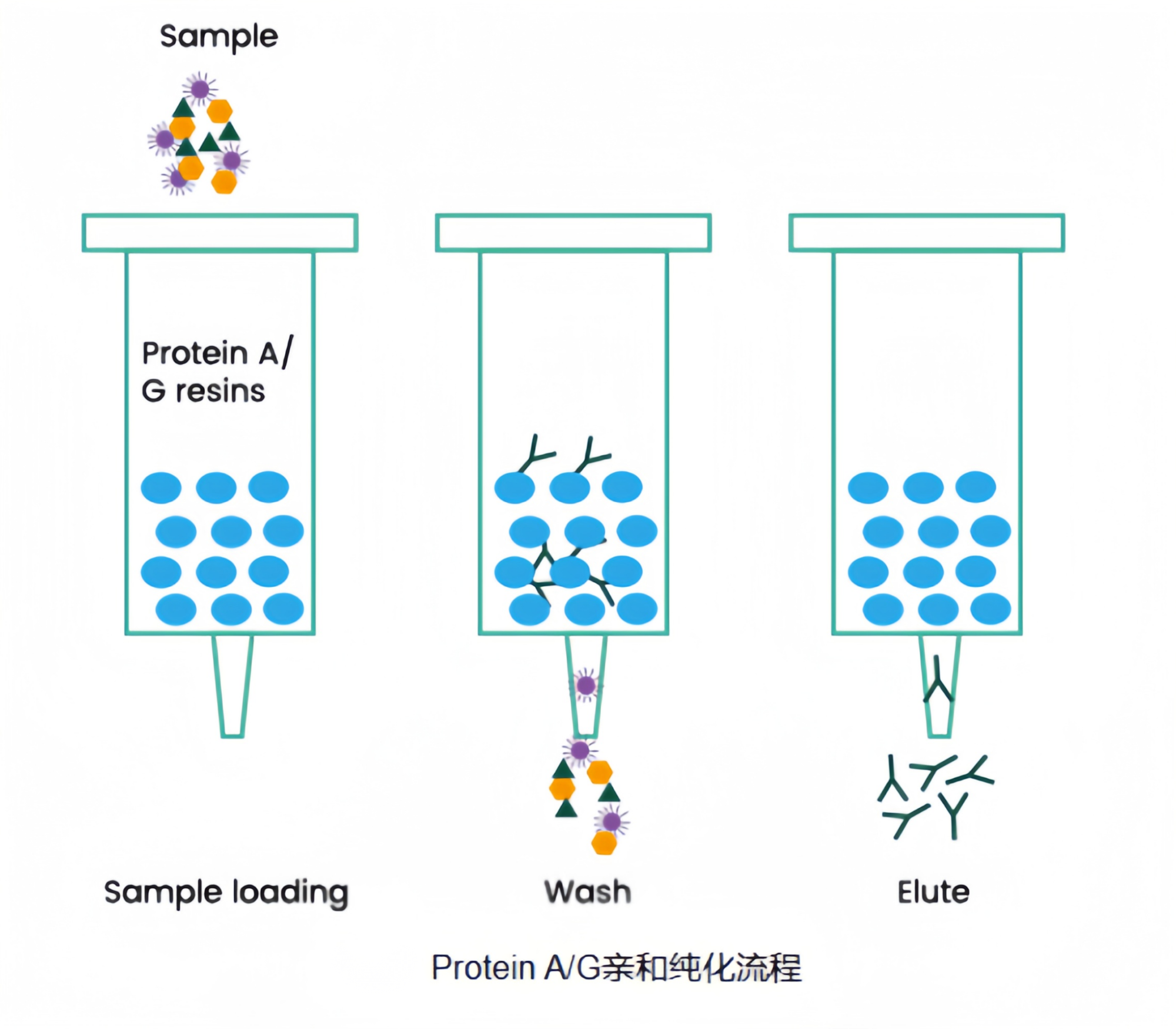
多抗亲和层析纯化技术流程
一、样品预处理阶段
1、 生物样品采集与初步处理
样品类型:涵盖血清(牛 / 兔 / 羊等多物种)、腹水(杂交瘤细胞)、重组细胞培养上清(CHO/HEK293 等工程细胞)
预处理操作:
血清 / 腹水:5000g 离心 30 分钟,去除细胞碎片及凝血块,取上清液
细胞上清:0.45μm 滤膜过滤,去除细胞残片及大颗粒杂质
缓冲液平衡:通过 PD-10 脱盐柱置换为中性缓冲液(如 PBS pH7.4 或 Tris-HCl pH7.5),消除原样品中盐分 / 防腐剂对层析的干扰
2. 样品质量控制
蛋白浓度测定:采用 BCA 法或 Bradford 法,确保上样浓度在 1-5mg/mL
杂质检测:SDS-PAGE 电泳初步评估杂蛋白种类及含量,避免过高杂质影响层析效率
二、亲和层析核心纯化阶段
1. 层析柱准备与配基固定化
(1)层析介质活化
常用填料:4B 琼脂糖凝胶(实验室级)、磁珠基填料(自动化高通量)、聚丙烯酰胺微球(工业级)
活化方法:氨基配基:CNBr 活化法(琼脂糖凝胶),通过溴化氰活化羟基生成亚氨基碳酸酯基团,偶联抗原 / 抗体氨基
羧基配基:NHS-EDC 法(通用型),通过 N - 羟基琥珀酰亚胺和 1 - 乙基 - 3-(3 - 二甲基氨基丙基)碳二亚胺活化羧基,形成活性酯键结合氨基基团
配基偶联:抗原 / 抗体浓度:5-15mg/mL 填料,室温振荡偶联 2-4 小时
偶联效率验证:BCA 法检测偶联后上清液蛋白残留,确保偶联率>90%
(2)样品上样与杂质洗脱
上样条件:
流速:1-2mL/min(实验室级)/ 5-10mL/min(工业级)
上样量:≤柱体积 10%(避免配基饱和导致漏样)
平衡洗杂:
缓冲液:10 倍柱体积(CV)的 PBS 或 TBS,去除未结合的杂蛋白
监测指标:紫外检测器(280nm)信号回落至基线,确认杂蛋白洗脱完全
(3)目标抗体洗脱
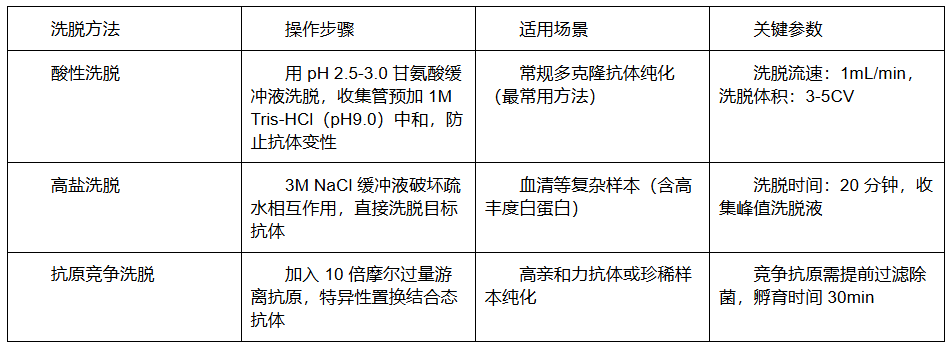
三、后处理与质量控制阶段
1. 洗脱液初步处理中和与浓缩:
酸性洗脱液立即用 Tris-HCl 中和至 pH7.0-7.5
超滤离心管(10kDa 截留分子量)浓缩至 5-10mg/mL,去除低分子量杂质
缓冲液置换:透析袋(截留分子量 30kDa)4℃过夜,置换为目标缓冲液(如含 5% 甘油的 PBS)
2. 质量检测核心项目
(1)纯度检测SDS-PAGE 银染:单一主条带,灰度分析显示纯度≥95%
尺寸排阻色谱(SEC-HPLC):主峰面积占比>98%,聚合体及降解产物<2%
(2)活性检测
ELISA 效价:间接法测定抗体效价≥1:10⁵(以包被抗原浓度 1μg/mL 计)
表面等离子共振(SPR):亲和常数 KD≤10⁻⁹M,确保抗体结合活性未受纯化影响
(3)安全性指标
内毒素检测:鲎试剂法<0.2EU/mg(适用于体内实验 / 诊断试剂)
微生物污染:培养法检测<10CFU/mL(无菌制剂需<1CFU/mL)
3. 成品处理无菌过滤:0.22μm 膜过滤分装,-20℃或 - 80℃冻存(添加 0.05% 叠氮钠防止污染)
标签标注:注明抗体名称、纯度、效价、批号、制备日期及储存条件
四、流程优化与关键控制点
1. 工艺参数优化策略配基密度优化:通过正交实验确定最佳偶联浓度(推荐 8-12mg 抗原 /mL 填料),平衡结合容量与特异性
洗脱梯度设计:复杂样本采用梯度洗脱(如 pH 从 7.4 逐步降至 2.8),减少非特异性洗脱带来的活性损失
2. 常见问题解决方案
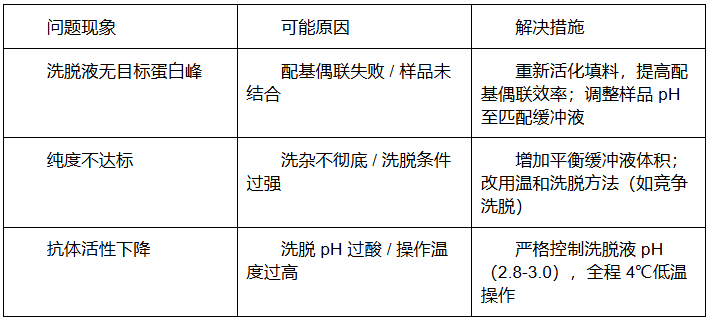
通过标准化操作流程与精准的参数控制,多抗亲和层析纯化技术可实现从复杂生物样品中高效获取高纯度、高活性的多克隆抗体,满足基础研究、诊断试剂开发及抗体药物生产的多样化需求。如需针对特定抗体类型(如鸡 IgY、羊驼纳米抗体)设计专属纯化方案,可联系技术团队获取定制化工艺路线。
